
Fel vid sterilisering av medicintekniska produkter kostar tillverkarna miljontals kronor varje år, och 15-20% av felen beror på otillräcklig ventilation som förhindrar att steriliseringsmedlet tränger in ordentligt. Standardventilationspluggar misslyckas under autoklav1 temperaturer på 121-134°C eller försämras när de utsätts för sterilisering med etylenoxid (ETO)2 kemikalier, vilket äventyrar sterilitetssäkringen och efterlevnaden av regelverket.
Steriliserbara ventilationspluggar möjliggör effektiv sterilisering genom att tillåta ång- eller ETO-gasinträngning samtidigt som sterila barriärer bibehålls efter sterilisering. Ventilationsöppningar med PTFE-membran tål autoklavtemperaturer på upp till 150 °C och motstår kemisk nedbrytning av ETO, vilket säkerställer tillförlitligt sterilitetsunderhåll för medicintekniska produkter, farmaceutisk utrustning och laboratorieinstrument som kräver validerade steriliseringsprocesser.
Förra året arbetade jag med Dr. Sarah Mitchell, kvalitetschef på en ledande tillverkare av medicintekniska produkter i Boston, som hade problem med steriliseringsvalideringen av sina förpackningar för implanterbara produkter. Deras standardventilationspluggar i nylon smälte under autoklavcyklerna och hindrade ångan från att tränga in ordentligt. Efter att ha bytt till våra steriliserbara ventilationspluggar av PTFE av farmaceutisk kvalitet med validerad temperaturbeständighet uppnådde de 100% steriliseringseffekt över 1 000 valideringscykler - vilket säkerställer FDA-efterlevnad och patientsäkerhet! 🏥
Innehållsförteckning
- Vad är steriliserbara ventilationsproppar och varför är de så viktiga?
- Hur påverkar olika steriliseringsmetoder materialet i ventilationspluggar?
- Vilka material är bäst för sterilisering i autoklav?
- Vilka material fungerar bäst för ETO-steriliseringsprocesser?
- Hur väljer och validerar du steriliserbara ventilationsproppar?
- Vanliga frågor om steriliserbara ventilationsproppar
Vad är steriliserbara ventilationsproppar och varför är de så viktiga?
Att förstå den roll som steriliserbara ventilationspluggar spelar i tillverkningen av medicintekniska produkter och läkemedel är avgörande för att upprätthålla sterilitetssäkring och regelefterlevnad.
Steriliserbara ventilationspluggar är specialiserade ventiler som andas och är utformade för att klara steriliseringsprocesser samtidigt som de tillåter steriliseringsmedel att tränga in och upprätthåller sterila barriärer. De möjliggör luftförskjutning under sterilisering, förhindrar vakuumbildning under kylning och upprätthåller sterila förhållanden efter sterilisering. Viktiga användningsområden är förpackningar för medicintekniska produkter, läkemedelsbehållare, laboratorieutrustning och utrustning för sterilisering.
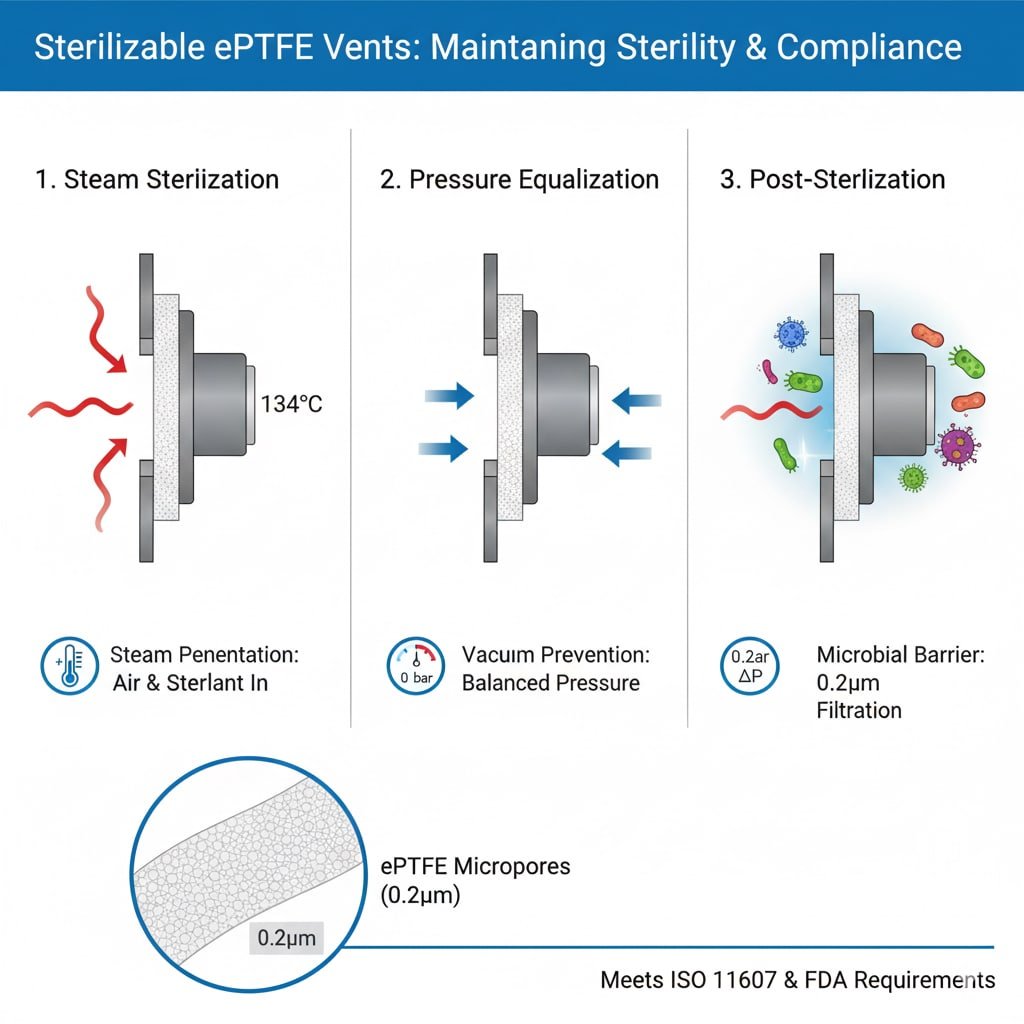
Krav på steriliseringsprocessen
Ångpenetration: Autoklavsterilisering kräver att ånga tränger in i förpackningen och kommer i kontakt med alla ytor, vilket kräver ventiler som tillåter gasflöde samtidigt som mikrobiella barriärer upprätthålls.
Luftförskjutning: För effektiv sterilisering krävs att luften avlägsnas helt och ersätts med steriliseringsmedel, vilket underlättas genom kontrollerat gasutbyte.
Tryckutjämning: Steriliseringscykler skapar tryckskillnader som ventilerna måste kunna hantera utan att äventyra de sterila barriärerna eller förpackningens integritet.
Kritiska prestandaparametrar
Temperaturbeständighet: Steriliserbara ventiler måste bibehålla strukturell integritet och filtreringsprestanda vid steriliseringstemperaturer från 121°C till 150°C.
Kemisk kompatibilitet: Materialen måste motstå nedbrytning från steriliseringskemikalier, t.ex. ånga, etylenoxid, väteperoxid och ozon.
Mikrobiell barriäreffektivitet: Efter sterilisering måste ventilerna ge en tillförlitlig mikrobiell barriär3 med porstorlekar på typiskt 0,2-0,22 mikrometer för kvarhållande av bakterier.
Överväganden om regelefterlevnad
FDA:s valideringskrav: Medicintekniska tillämpningar kräver validerade steriliseringsprocesser med dokumenterad ventilationsprestanda under hela steriliseringscykeln.
Överensstämmelse med ISO-standarder: Steriliserbara ventilationsöppningar måste uppfylla ISO 116074 förpackningsstandarder och ISO 17665 ångsteriliseringskrav för medicinska tillämpningar.
Test av biokompatibilitet: Applikationer med kontakt med medicintekniska produkter kan kräva USP Class VI biokompatibilitetstest för att garantera patientsäkerheten.
Applikationskategorier
Förpackningar för medicintekniska produkter: Sterila förpackningar för implantat, kirurgiska instrument och medicintekniska produkter för engångsbruk som kräver bibehållen sterilitet fram till användning.
Läkemedelstillverkning: Steril processutrustning, bioreaktorer och läkemedelsbehållare som kräver validerade steriliseringsprocesser.
Laboratorieutrustning: Autoklaverbara laboratoriebehållare, odlingskärl och analysutrustning som kräver sterila förhållanden för korrekta resultat.
Hur påverkar olika steriliseringsmetoder materialet i ventilationspluggar?
Olika steriliseringsmetoder skapar unika utmaningar för material till ventpluggar, vilket kräver specifika materialegenskaper och designöverväganden för optimal prestanda.
Vid ångsterilisering utsätts materialet för höga temperaturer (121-134 °C) och mättad ånga som kan orsaka termisk nedbrytning, dimensionsförändringar och membranskador. ETO-sterilisering utsätter materialen för reaktiva kemikalier vid lägre temperaturer (37-63 °C) men längre exponeringstider som kan orsaka kemisk nedbrytning och avgasning. Varje metod kräver specifika materialval för att ge tillförlitlig prestanda.
Effekter av ångsterilisering
Termisk stress: Höga temperaturer orsakar termisk expansion, potentiell smältning av termoplastiska komponenter och nedbrytning av temperaturkänsliga material.
Hydrolysreaktioner5: Exponering för ånga kan orsaka hydrolytisk nedbrytning av vissa polymerer, särskilt polyestrar och vissa polyamider.
Dimensionell stabilitet: Upprepad termisk cykling kan orsaka dimensionella förändringar som påverkar tätningsprestanda och filtreringseffektivitet.
Utmaningar vid ETO-sterilisering
Kemisk reaktivitet: Etylenoxid reagerar med material som innehåller aktiva väteatomer, vilket kan förändra materialegenskaperna och skapa giftiga restprodukter.
Krav på avgasning: ETO-steriliserade produkter kräver längre luftningsperioder för att avlägsna absorberad ETO och reaktionsprodukter innan de kan användas på ett säkert sätt.
Penetrationsegenskaper: ETO kräver specifika fuktighets- och temperaturförhållanden för effektiv penetration, vilket påverkar kraven på ventilationsutformning.
Väteperoxid Plasmaeffekter
Oxidativ nedbrytning: H2O2-plasma skapar mycket reaktiva ämnen som kan bryta ned organiska material genom oxidationsreaktioner.
Materialkompatibilitet: Många elastomerer och vissa plaster är inte kompatibla med H2O2 plasmasterilisering på grund av snabb nedbrytning.
Fördelar vid låga temperaturer: Plasmasterilisering sker vid låga temperaturer (45-55°C), vilket minskar den termiska belastningen på temperaturkänsliga material.
Överväganden om gammastrålning
Strålningsskada: Gammastrålning med hög energi kan orsaka klyvning eller tvärbindning av polymerkedjor, vilket avsevärt förändrar materialegenskaperna.
Ackumulering av doser: Upprepad gammasterilisering kan orsaka kumulativa skador, vilket begränsar antalet steriliseringscykler som materialen tål.
Krav på antioxidanter: Strålningsresistenta formuleringar kräver ofta antioxidanter för att förhindra oxidativ nedbrytning under och efter bestrålning.
Jag hjälpte nyligen Ahmed Al-Rashid, driftchef på en läkemedelsanläggning i Dubai, att lösa valideringsproblem med ETO-sterilisering i deras ventilationssystem för bioreaktorer. Deras standardventilationspluggar absorberade ETO och krävde förlängda 14-dagars luftningsperioder som störde produktionsscheman. Genom att implementera våra ETO-kompatibla PTFE-ventilationspluggar med minimala absorptionsegenskaper minskade de luftningstiden till 24 timmar samtidigt som de upprätthöll full sterilitetssäkring - vilket dramatiskt förbättrade produktionseffektiviteten! 🚀
Vilka material är bäst för sterilisering i autoklav?
För att välja lämpliga material för autoklavsterilisering måste man förstå termisk stabilitet, hydrolysbeständighet och långsiktig prestanda under upprepad ångexponering.
PTFE (polytetrafluoretylen) ger överlägsen autoklavprestanda med kontinuerliga drifttemperaturer upp till 260°C, utmärkt kemisk inertitet och hydrolysbeständighet. PVDF (polyvinylidenfluorid) ger god termisk stabilitet till 150°C till lägre kostnad. Undvik nylon, standardpolyeten och de flesta elastomerer som bryts ned under autoklavförhållanden, vilket försämrar filtrerings- och tätningsprestanda.
Fördelar med PTFE-membran
Exceptionell temperaturbeständighet: PTFE bibehåller strukturell integritet och filtreringsprestanda vid temperaturer som ligger långt över typiska autoklavförhållanden (121-134°C).
Kemisk inertitet: PTFE motstår nedbrytning från ånga, rengöringskemikalier och biprodukter från sterilisering, vilket ger en jämn och långsiktig prestanda.
Hydrofoba egenskaper: PTFE:s hydrofoba egenskaper förhindrar vattenabsorption och bibehåller dimensionsstabiliteten under alla steriliseringscykler.
Jämförelse av materialprestanda
| Material | Max temperatur (°C) | Motstånd mot ånga | Hydrolysresistens | Kostnadsfaktor |
|---|---|---|---|---|
| PTFE | 260 | Utmärkt | Utmärkt | Hög |
| PVDF | 150 | Bra | Bra | Medium |
| PP (Polypropylen) | 135 | Rättvist | Rättvist | Låg |
| Nylon | 80-100 | Dålig | Dålig | Låg |
Val av material för hölje
Rostfritt stål 316L: Ger utmärkt korrosionsbeständighet, termisk stabilitet och rengörbarhet för farmaceutiska och medicinska tillämpningar som kräver validerade rengöringsrutiner.
PEEK (polyeteretereterketon): Ger enastående termisk stabilitet (kontinuerlig användning till 250°C) med utmärkt kemisk beständighet för krävande autoklavtillämpningar.
Polypropylen: Kostnadseffektivt alternativ för engångsapplikationer med tillräcklig prestanda för standardautoklavcykler vid 121°C.
Överväganden om tätningskomponenter
EPDM O-ringar: Ger god ångbeständighet och termisk stabilitet för temperaturer upp till 150°C med utmärkt tätningsprestanda.
Silikontätningar: Ger överlägsen temperaturbeständighet (upp till 200°C) men kan ha kompatibilitetsproblem med vissa rengöringskemikalier.
PTFE-inkapslade O-ringar: Kombinera PTFE:s kemiska beständighet med elastomertätningsegenskaper för krävande applikationer som kräver båda dessa egenskaper.
Designoptimering för användning i autoklav
Termisk expansionsförmåga: Ventilationsutformningen måste ta hänsyn till den differentiella värmeutvidgningen mellan materialen för att förhindra att tätningen går sönder vid temperaturväxlingar.
Dräneringsfunktioner: Korrekt utformning av dräneringen förhindrar ansamling av kondensat som kan försämra filtreringsprestandan eller skapa kontamineringsrisker.
Stöd för validering: Konstruktionsdetaljerna ska underlätta valideringstestning, inklusive tryckfall, mikrobiell utmaning och verifiering av termisk prestanda.
Vilka material fungerar bäst för ETO-steriliseringsprocesser?
ETO-sterilisering innebär unika materialutmaningar som kräver kemisk kompatibilitet, minimal absorption och snabba utgasningsegenskaper för effektiv bearbetning.
PTFE och PVDF ger utmärkt ETO-kompatibilitet med minimal kemisk absorption och snabb avgasning. Undvik material med aktiva vätesiter som nylon, PVC och naturgummi som reagerar med ETO och bildar giftiga föreningar. Höljen av rostfritt stål ger optimal kemisk beständighet, medan silikontätningar ger god ETO-kompatibilitet med acceptabla avgasningsegenskaper för de flesta applikationer.
ETO:s kemiska kompatibilitet
Reaktionsmekanismer: ETO reagerar med material som innehåller hydroxyl-, amino-, karboxyl- och sulfhydrylgrupper och bildar etylenglykolderivat och andra potentiellt giftiga föreningar.
Absorptionsegenskaper: Material med hög ETO-absorption kräver längre luftningsperioder, vilket ökar bearbetningstiden och kostnaderna avsevärt.
Kinetik för avgasning: Material med snabb avgasning möjliggör kortare luftningscykler, vilket förbättrar processeffektiviteten och minskar lagerhållningstiden.
Rankning av ETO-prestanda för material
Utmärkt ETO-kompatibilitet:
- PTFE: Minimal absorption, snabb avgasning, ingen kemisk reaktivitet
- PVDF: Låg absorption, god avgasning, utmärkt kemisk beständighet
- Rostfritt stål: Ingen absorption, omedelbar användbarhet
God ETO-kompatibilitet:
- Polypropylen: Måttlig absorption, acceptabel avgasning
- Silikon: Låg reaktivitet, måttliga krav på avgasning
Dålig ETO-kompatibilitet:
- Nylon: Hög reaktivitet, långvarig luftning krävs
- PVC: Kemisk nedbrytning, bildning av toxiska föreningar
- Naturgummi: Hög absorption, potentiell nedbrytning
Krav på luftningstid
| Material | Typisk luftningstid | ETO Absorptionsnivå | Utgasningshastighet |
|---|---|---|---|
| PTFE | 8-24 timmar | Minimal | Snabb |
| PVDF | 24-48 timmar | Låg | Bra |
| Polypropylen | 48-72 timmar | Måttlig | Måttlig |
| Nylon | 7-14 dagar | Hög | Långsam |
Optimering av processparametrar
Temperaturkontroll: ETO-sterilisering sker vanligtvis vid 37-63°C, vilket kräver material som bibehåller prestanda i hela detta temperaturintervall.
Krav på luftfuktighet: För att ETO ska fungera krävs en relativ luftfuktighet på 40-80%, vilket kräver material som fungerar konsekvent under dessa fuktförhållanden.
Hantering av gaskoncentration: ETO-koncentrationer på 450-1200 mg/L kräver material som motstår kemiska angrepp samtidigt som de tillåter steriliseringsmedlet att tränga in.
Överväganden om validering
Testning av restprodukter: ETO-steriliserade produkter måste testas för ETO-rester och reaktionsprodukter för att säkerställa att säkerhetsgränserna följs.
Biokompatibilitet Underhåll: Materialen måste bibehålla sin biokompatibilitet efter ETO-exponering och luftning, vilket kräver validerade materialval.
Processövervakning: ETO-sterilisering kräver kontinuerlig övervakning av temperatur, luftfuktighet, tryck och gaskoncentration under hela cykeln.
Hur väljer och validerar du steriliserbara ventilationsproppar?
Korrekt val och validering av steriliserbara ventilationspluggar säkerställer tillförlitlig steriliseringsprestanda, efterlevnad av regelverk och långsiktig driftsframgång.
Vid val av material måste man matcha materialegenskaperna med steriliseringsmetoden, definiera prestandakrav och beakta lagstadgade standarder. Validering omfattar termisk prestandatestning, studier av mikrobiell påverkan, bedömning av kemisk kompatibilitet och utvärdering av långtidsstabilitet. Dokumentera alla tester i enlighet med FDA- och ISO-standarder för inlämning av registreringshandlingar och efterlevnad av kvalitetssystem.
Ramverk för urvalskriterier
Steriliseringsmetod Kompatibilitet: Anpassa ventilationsmaterial till specifika steriliseringsmetoder (ånga, ETO, H2O2-plasma, gamma) baserat på krav på temperatur, kemikalie- och strålningsbeständighet.
Specifikationer för prestanda: Definiera erforderliga flödeshastigheter, tryckklassningar, filtreringseffektivitet och mikrobiella barriäregenskaper baserat på applikationskrav.
Lagstadgade krav: Tänk på FDA:s produktklassificering, överensstämmelse med ISO-standarder och krav på biokompatibilitet för avsedda användningsområden.
Parametrar för bedömning av ansökan
Driftsmiljö: Utvärdera temperaturintervall, kemisk exponering, tryckförhållanden och kontamineringsrisker under produktens hela livscykel.
Steriliseringsfrekvens: Överväg engångsbruk kontra flera steriliseringscykler och kumulativa effekter på materialets prestanda och tillförlitlighet.
Valideringens omfattning: Fastställa testkrav baserat på riskbedömning, regelverk och krav på kvalitetssystem.
Protokoll för valideringstestning
Test av termisk prestanda:
- Temperaturcykling vid steriliseringsförhållanden
- Mätning av dimensionell stabilitet
- Verifiering av filtreringseffektivitet efter termisk exponering
Testning av mikrobiell utmaning:
- Bakterieutmaning med lämpliga testorganismer
- Verifiering av upprätthållande av sterilitet
- Bedömning av barriärens integritet på lång sikt
Bedömning av kemisk kompatibilitet:
- Utvärdering av materialnedbrytning
- Testning av extraherbara och lakbara ämnen
- Verifiering av underhåll av biokompatibilitet
Krav på dokumentation
Materialspecifikationer: Kompletta materialdatablad med kemisk sammansättning, termiska egenskaper och myndighetscertifieringar.
Testprotokoll: Detaljerade valideringsprotokoll enligt FDA:s riktlinjer och ISO-standarder för validering av sterilisering.
Prestationsdata: Omfattande testresultat som visar prestanda under specificerade driftsförhållanden och steriliseringscykler.
Integration av kvalitetssystem
Kvalificering av leverantör: Upprätta kvalitetsavtal med leverantörer, inklusive krav på materialspårbarhet, ändringskontroll och kvalitetsdokumentation.
Inkommande inspektion: Utveckla inspektionsförfaranden för verifiering av kritiska dimensioner, materialegenskaper och prestandaegenskaper.
Validering av processer: Integrera ventilationsprestanda i den övergripande valideringen av steriliseringsprocessen, inklusive testning av värsta tänkbara scenario.
Överväganden om riskhantering
Failure Mode Analysis: Identifiera potentiella felmoder, inklusive materialnedbrytning, tätningsfel och filtreringskompromiss med lämpliga begränsningsstrategier.
Förändringskontroll: Fastställ rutiner för hantering av materialändringar, leverantörsändringar och ändringar av specifikationer med lämpliga krav på förnyad validering.
Kontinuerlig övervakning: Implementera löpande övervakningsprogram för att verifiera fortsatt prestanda och identifiera potentiella problem innan de påverkar produktkvaliteten.
Slutsats
Steriliserbara ventilationspluggar spelar en avgörande roll för att säkerställa effektiv sterilisering och samtidigt upprätthålla sterila barriärer i medicintekniska och farmaceutiska tillämpningar. Att förstå de unika utmaningarna med olika steriliseringsmetoder och välja lämpliga material är avgörande för tillförlitlig prestanda och regelefterlevnad.
PTFE-baserade ventilationspluggar ger överlägsen prestanda i flera olika steriliseringsmetoder och ger utmärkt temperaturbeständighet, kemisk kompatibilitet och långsiktig tillförlitlighet. Rätt val och validering säkerställer optimal steriliseringseffektivitet samtidigt som behandlingstid och kostnader minimeras.
Bepto har ett omfattande sortiment av steriliserbara ventilationspluggar med PTFE-membran av farmaceutisk kvalitet, validerad temperaturprestanda och kompletta dokumentationspaket för regulatoriska ansökningar. Med över tio års erfarenhet av specialiserade ventilationsapplikationer och ISO-certifierad tillverkningskapacitet erbjuder vi de tillförlitliga och kostnadseffektiva lösningar du behöver för kritiska steriliseringsapplikationer. Lita på att vi håller dina steriliseringsprocesser validerade och dina produkter säkra! 🔬
Vanliga frågor om steriliserbara ventilationsproppar
F: Kan samma ventilationsplugg användas för både autoklav- och ETO-sterilisering?
A: Ja, ventilationspluggar med PTFE-membran kan hantera både autoklav- och ETO-sterilisering effektivt. PTFE har utmärkt temperaturbeständighet för autoklavcykler och minimal ETO-absorption för snabb luftning, vilket gör den idealisk för anläggningar som använder flera steriliseringsmetoder.
F: Hur många steriliseringscykler klarar en ventilationsplugg?
A: Högkvalitativa PTFE-ventilationspluggar klarar normalt 100+ autoklavcykler eller 50+ ETO-cykler med bibehållen filtreringsprestanda. Den faktiska cykeltiden beror på steriliseringsparametrar, hanteringsprocedurer och kriterier för godkännande av prestanda för din specifika applikation.
F: Vilken porstorlek krävs för sterilfiltrering i medicinska tillämpningar?
A: Medicinska applikationer kräver vanligtvis porstorlekar på 0,2 eller 0,22 mikrometer för tillförlitlig bakterieavskiljning. Denna porstorlek ger validerad sterilitetssäkring samtidigt som den tillåter tillräckligt gasflöde för effektiv sterilisering och tryckutjämning.
F: Kräver steriliserbara ventilationspluggar särskilda valideringstester?
A: Ja, steriliserbara ventilationspluggar kräver valideringstestning, inklusive termisk prestanda, mikrobiell utmaning och studier av materialkompatibilitet. Testerna måste följa FDA:s riktlinjer och ISO-standarder, och dokumentationen ska stödja valideringen av steriliseringsprocessen och de regulatoriska ansökningarna.
F: Hur förhindrar man kontaminering av ventilationspluggen under sterilisering?
A: Förhindra kontaminering genom korrekt installation, skyddshöljen under hantering, validerade steriliseringsparametrar och lämplig förvaring efter sterilisering. Använd steril teknik under installationen och se till att ventilationspluggarna är utformade för din specifika steriliseringsmetod och dina applikationskrav.
Lär dig de vetenskapliga principerna för autoklavsterilisering och hur mättad ånga under tryck används för att effektivt döda mikroorganismer. ↩
Utforska den kemiska processen för sterilisering med etylenoxid (ETO), en lågtemperaturmetod som används för att sterilisera värme- och fuktkänsliga medicintekniska produkter. ↩
Upptäck de metoder som används för att testa och validera effektiviteten hos en mikrobiell barriär, för att säkerställa att den förhindrar inträngning av mikroorganismer och bibehåller steriliteten. ↩
Gå igenom de viktigaste kraven i standarden ISO 11607, som specificerar material och provning för sterila barriärsystem för medicintekniska produkter. ↩
Förstå den kemiska reaktionen hydrolys och hur den kan orsaka nedbrytning av vissa polymera material när de utsätts för vatten eller ånga vid höga temperaturer. ↩


