
醫療裝置滅菌失敗每年造成製造商數以百萬計的損失,其中 15-20% 的失敗歸咎於排氣不足,導致滅菌劑無法正常滲透。標準排氣塞在下列情況下會失效 壓力鍋1 溫度為 121-134°C 或暴露於下列環境時會降解 環氧乙烷 (ETO) 滅菌2 化學品,影響無菌保證和法規遵循。
可滅菌透氣塞可讓蒸氣或 ETO 氣體滲透,同時維持滅菌後的無菌屏障,從而達到有效的滅菌效果。PTFE 膜排氣孔可承受高達 150°C 的高壓滅菌溫度,並可抵抗 ETO 化學降解,確保需要有效滅菌程序的醫療裝置、製藥設備和實驗室儀器能可靠地維持無菌狀態。
去年,我與波士頓一家領先醫療設備製造商的品質主管 Sarah Mitchell 博士合作,他們的植入式設備包裝遇到了滅菌驗證失敗的問題。他們的標準尼龍通氣塞在高壓滅菌週期中熔化,阻礙了蒸汽的正常滲透。在改用我們具有經驗證耐高溫的藥用級 PTFE 滅菌通氣塞後,他們在 1,000 次驗證週期中達到了 100% 的滅菌效果 - 確保符合 FDA 規範和患者安全!🏥
目錄
什麼是可滅菌通風塞,為什麼它們很重要?
瞭解可滅菌排氣塞在醫療器材和製藥過程中的作用,對於維持無菌保證和符合法規要求至關重要。
可滅菌透氣塞是專門設計的透氣透氣孔,可承受滅菌過程,同時允許滅菌劑滲透並保持無菌屏障。它們可以在滅菌過程中排出空氣,在冷卻過程中防止真空形成,並在滅菌後保持無菌狀態。關鍵應用包括醫療裝置包裝、藥物容器、實驗室設備和無菌加工設備。
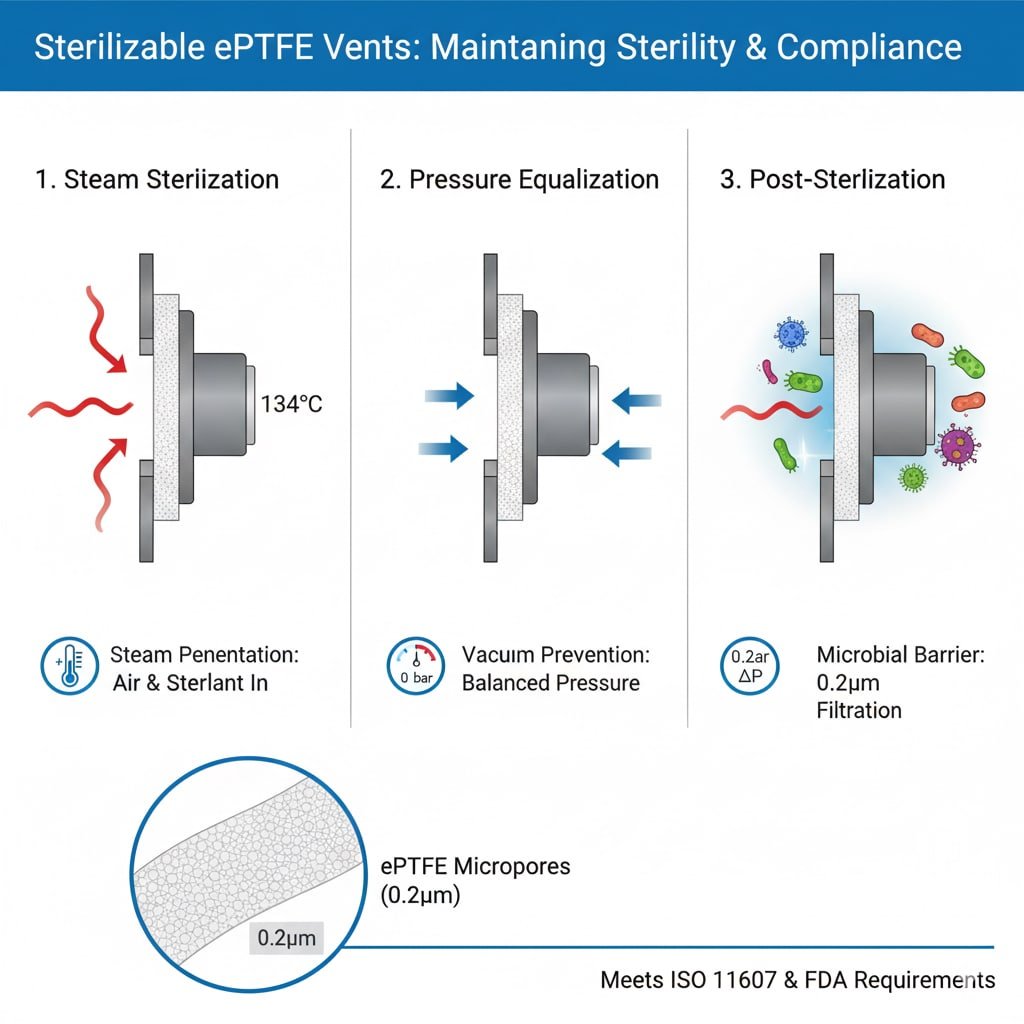
滅菌製程要求
蒸氣滲透: 高壓滅菌需要蒸氣滲透包裝並接觸所有表面,因此需要既能讓氣體流動又能保持微生物屏障的通風口。
排氣量: 有效的滅菌需要完全排出空氣並用滅菌劑替換,而通風口可透過控制氣體交換來達到此目的。
壓力平衡: 滅菌週期會產生壓力差,通風口必須能夠適應壓力差,而不影響滅菌屏障或包裝的完整性。
關鍵性能參數
耐溫性: 可滅菌通風口必須在 121°C 至 150°C 的滅菌溫度下保持結構完整性和過濾性能。
化學相容性: 材料必須能抵抗消毒化學物質的降解,包括蒸氣、環氧乙烷、過氧化氫和臭氧。
微生物屏障效率: 消毒後,通風口必須提供可靠的 微生物屏障3 其孔隙大小通常為 0.2-0.22 微米,用於保留細菌。
法規遵循考量
FDA 驗證要求: 醫療設備應用需要經過驗證的滅菌流程,並在整個滅菌週期中記錄通風口性能。
符合 ISO 標準: 可消毒通風口必須符合 ISO 116074 包裝標準和醫療應用的 ISO 17665 蒸氣消毒要求。
生物相容性測試: 醫療裝置接觸應用可能需要進行 USP Class VI 生物相容性測試,以確保病患安全。
應用類別
醫療器材包裝: 用於植入物、手術器械和使用前需保持無菌狀態的一次性醫療裝置的無菌包裝。
製藥: 無菌加工設備、生物反應器和需要經過驗證的滅菌製程的藥用容器。
實驗室設備: 可高壓滅菌的實驗室容器、培養器皿和需要無菌條件以獲得準確結果的分析設備。
不同的滅菌方法如何影響通風塞材料?
不同的滅菌方法會對通風孔塞子材料造成獨特的挑戰,需要特定的材料特性和設計考量才能達到最佳效能。
蒸氣滅菌將材料置於高溫(121-134°C)和飽和蒸氣條件下,可能導致熱降解、尺寸變化和膜損壞。ETO 滅菌會讓材料暴露在較低溫度 (37-63°C) 的活性化學物質中,但暴露時間較長,可能會造成化學降解和排氣。每種方法都需要特定的材料選擇以獲得可靠的性能。
蒸氣消毒效果
熱應力: 高溫會導致熱膨脹、熱塑性元件可能熔化,以及對溫度敏感的材料降解。
水解反應5: 蒸氣曝露會導致某些聚合物水解降解,尤其是聚酯和某些聚酰胺。
尺寸穩定性: 重複的熱循環會造成尺寸變化,影響密封性能和過濾效率。
ETO 滅菌的挑戰
化學反應性: 環氧乙烷會與含有活性氫原子的材料發生反應,可能會改變材料特性並產生有毒殘留物。
除氣要求: 經 ETO 滅菌的產品需要較長的通氣期,以去除吸收的 ETO 和反應產物,才能安全使用。
穿透特性: ETO 需要特定的濕度和溫度條件才能有效滲透,因此會影響通風口的設計要求。
過氧化氫電漿效果
氧化降解: H2O2 等離子體可產生高活性物質,透過氧化反應降解有機材料。
材質相容性: 許多彈性體及某些塑膠因快速降解而與 H2O2 等離子體滅菌不相容。
低溫優勢: 等離子滅菌在低溫 (45-55°C) 下操作,可減少對溫度敏感材料的熱應力。
伽馬輻射注意事項
輻射損害: 高能量的伽馬輻射會造成聚合物鏈裂開或交聯,顯著改變材料的特性。
劑量累積: 重複伽馬滅菌可能會造成累積性損害,限制材料可承受的滅菌循環次數。
抗氧化需求: 抗輻射配方通常需要抗氧化劑來防止輻射期間及之後的氧化降解。
我最近幫助迪拜一家製藥廠的營運經理 Ahmed Al-Rashid 解決了他們生物反應器通風系統的 ETO 滅菌驗證問題。他們的標準通氣塞吸收了 ETO,需要長達 14 天的通氣期,打亂了生產計劃。透過採用我們具有最小吸收特性的 ETO 相容 PTFE 通氣塞,他們將通氣時間縮短至 24 小時,同時維持完全的無菌保證 - 大幅提高生產效率!🚀
哪些材料最適合高壓滅菌?
要為高壓滅菌選擇合適的材料,必須瞭解材料的熱穩定性、耐水解性,以及在重複蒸汽暴露下的長期性能。
PTFE (聚四氟乙烯) 具備優異的高壓滅菌性能,連續使用溫度可達 260°C,並具有極佳的化學惰性和耐水解性。PVDF(聚偏氟乙烯)具有良好的熱穩定性,可達 150°C,且成本較低。避免使用尼龍、標準聚乙烯和大多數彈性材料,因為它們會在高壓滅菌條件下降解,影響過濾和密封性能。
PTFE 膜的優勢
卓越的耐溫性: PTFE 可在遠高於典型高壓滅菌條件 (121-134°C) 的溫度下保持結構完整性和過濾性能。
化學惰性: PTFE 可抵抗蒸氣、清潔化學品和滅菌副產品的降解,確保長期穩定的性能。
疏水特性: PTFE 的疏水性可防止吸水,並在整個消毒週期中保持尺寸穩定。
材料性能比較
| 材質 | 最高溫度 (°C) | 蒸汽阻力 | 耐水解性 | 成本因素 |
|---|---|---|---|---|
| PTFE | 260 | 極佳 | 極佳 | 高 |
| PVDF | 150 | 良好 | 良好 | 中型 |
| PP(聚丙烯) | 135 | 公平 | 公平 | 低 |
| 尼龍 | 80-100 | 貧窮 | 貧窮 | 低 |
外殼材料選擇
不銹鋼 316L: 具有優異的耐腐蝕性、熱穩定性和清潔性,適用於需要有效清潔程序的製藥和醫療應用。
PEEK(聚醚醚酮): 具有出色的熱穩定性(連續使用溫度可達 250°C)和卓越的耐化學性,適用於要求嚴苛的高壓滅菌應用。
聚丙烯: 適用於單次使用的高成本效益選項,其效能足以應付 121°C 的標準高壓滅菌循環。
密封元件注意事項
EPDM O 型環: 提供良好的耐蒸煮性及熱穩定性,適用溫度最高可達 150°C,密封性能極佳。
矽膠密封件: 提供優異的耐溫性(高達 200°C),但可能與某些清潔化學品有相容性問題。
PTFE 封裝 O 型環: 結合 PTFE 的耐化學性與彈性體的密封特性,適用於需要這兩種性能特性的嚴苛應用。
使用高壓滅菌器的設計優化
熱膨脹容納性: 排氣口設計必須顧及材料之間的熱膨脹差異,以防止在溫度循環過程中密封失效。
排水功能: 適當的排水設計可防止冷凝水積聚,以免影響過濾效能或造成污染風險。
驗證支援: 設計特點應有助於驗證測試,包括壓力衰減、微生物挑戰和熱績效驗證。
哪些材料最適合 ETO 滅菌製程?
ETO 滅菌提出了獨特的材料挑戰,要求化學相容性、最小吸收性和快速排氣特性,以達到高效處理。
PTFE 和 PVDF 具有極佳的 ETO 相容性,吸收化學物質最少,排氣速度快。避免使用尼龍、PVC 和天然橡膠等具有活躍氫位點的材料,這些材料會與 ETO 發生反應,形成有毒化合物。不銹鋼外殼具有最佳的耐化學性,而矽膠密封件則具有良好的 ETO 相容性,其放氣特性在大多數應用中都是可以接受的。
ETO 化學相容性
反應機制: ETO 會與含有羥基、氨基、羧基和巯基的材料發生反應,形成乙二醇衍生物和其他可能有毒的化合物。
吸收特性: 高 ETO 吸收率的材料需要延長曝氣時間,大幅增加製程時間與成本。
放氣動力學: 快速排氣材料可縮短曝氣週期,提高製程效率並縮短庫存保留時間。
材料 ETO 性能排名
優異的 ETO 相容性:
- PTFE:吸收量最小、排氣速度快、無化學反應性
- PVDF:低吸收性、良好的排氣性、優異的耐化學性
- 不銹鋼:無吸收性,可立即使用
良好的 ETO 相容性:
- 聚丙烯:適度吸收,可接受的放氣
- 矽膠:低反應性,中等放氣要求
ETO 兼容性差:
- 尼龍:高反應性,需要延長曝氣時間
- PVC: 化學降解、有毒化合物形成
- 天然橡膠:高吸收性、潛在降解
曝氣時間要求
| 材質 | 典型曝氣時間 | ETO 吸收水平 | 排氣率 |
|---|---|---|---|
| PTFE | 8-24 小時 | 最低限度 | 快速 |
| PVDF | 24-48 小時 | 低 | 良好 |
| 聚丙烯 | 48-72 小時 | 中度 | 中度 |
| 尼龍 | 7-14 天 | 高 | 慢速 |
製程參數最佳化
溫度控制: ETO 滅菌通常在 37-63°C 的溫度下運作,因此需要材料能在此溫度範圍內維持效能。
濕度要求: ETO 的有效性需要 40-80% 的相對濕度,因此必須使用在這些濕度條件下性能穩定的材料。
氣體濃度管理: 450-1200 mg/L 的 ETO 濃度要求材料既能抵抗化學侵蝕,又能滲透消毒劑。
驗證注意事項
殘留物測試: 經 ETO 滅菌的產品需要進行 ETO 殘留物和反應產物的測試,以確保符合安全限制。
生物相容性維護: 材料必須在 ETO 曝露和通氣後維持生物相容性,因此需要經過驗證的材料選擇。
製程監控: ETO 滅菌需要在整個週期內持續監控溫度、濕度、壓力和氣體濃度。
如何選擇和驗證可消毒的通風塞?
正確選擇和驗證可滅菌的排氣塞,可確保可靠的滅菌性能、符合法規要求和長期運作成功。
選擇時需要將材料特性與滅菌方法相匹配,定義性能要求,並考慮監管標準。驗證包括熱性能測試、微生物挑戰研究、化學相容性評估和長期穩定性評估。根據 FDA 和 ISO 標準記錄所有測試,以便提交監管申請和符合品質系統要求。
篩選標準架構
滅菌方法相容性: 根據溫度、化學和抗輻射要求,將通風口材料與特定的消毒方法(蒸汽、ETO、H2O2 等離子體、伽馬)相匹配。
性能規格: 根據應用需求,定義所需的流量、壓力額定值、過濾效率和微生物阻隔特性。
法規要求: 考慮 FDA 裝置分類、ISO 標準符合性,以及預期用途應用的生物相容性要求。
應用評估參數
作業環境: 評估整個產品生命週期的溫度範圍、化學曝曬、壓力條件和污染風險。
滅菌頻率: 考慮單次使用與多次消毒週期,以及對材料性能和可靠性的累積影響。
驗證範圍: 根據風險評估、法規途徑和品質系統要求來確定測試要求。
驗證測試協議
熱性能測試:
- 消毒條件下的溫度循環
- 尺寸穩定性測量
- 熱暴露後的過濾效率驗證
微生物挑戰測試:
- 使用適當的測試生物進行細菌挑戰
- 無菌保持驗證
- 長期阻隔完整性評估
化學相容性評估:
- 材料降解評估
- 萃取物和浸出物測試
- 生物相容性維護驗證
文件要求
材質規格: 完整的材料資料表,包括化學成份、熱特性和法規認證。
測試規程: 遵循 FDA 指南和 ISO 滅菌驗證標準的詳細驗證協議。
績效資料: 全面的測試結果顯示在指定的操作條件和消毒週期中的性能。
品質系統整合
供應商資格: 建立供應商品質協議,包括材料可追溯性、變更控制和品質文件要求。
進廠檢查: 針對關鍵尺寸、材料特性和性能特徵驗證制定檢驗程序。
製程驗證: 將通風口性能整合到整體滅菌製程驗證中,包括最壞情況測試。
風險管理考慮因素
失效模式分析: 識別潛在故障模式,包括材料降解、密封失效和過濾損壞,並採取適當的緩解策略。
變更控制: 建立管理材料變更、供應商變更和規格修改的程序,並提出適當的重新驗證要求。
持續監控: 實施持續監控計畫,以驗證持續的效能,並在潛在問題影響產品品質前加以識別。
總結
可滅菌透氣塞在確保有效滅菌,同時維持醫療器材和製藥應用中的無菌屏障方面扮演著重要角色。瞭解不同滅菌方法所面臨的獨特挑戰,並選擇合適的材料,對於可靠的性能和符合法規要求至關重要。
以 PTFE 為基礎的排氣塞在多種滅菌方法中都有優異的性能,提供出色的耐溫性、化學相容性和長期可靠性。正確的選擇和驗證可確保最佳的滅菌效果,同時將處理時間和成本降至最低。
在 Bepto,我們全面的可滅菌排氣塞包括藥用等級的 PTFE 膜、經驗證的溫度性能和完整的文件包,以滿足法規要求。憑藉十多年的專業排氣應用經驗和 ISO 認證製造能力,我們為您提供關鍵滅菌應用所需的可靠、具成本效益的解決方案。請相信我們能確保您的滅菌製程有效,產品安全!🔬
關於可消毒通風塞的常見問題
問:同樣的排氣塞可以用於高壓滅菌和 ETO 滅菌嗎?
A: 是的,PTFE 膜排氣塞可有效處理高壓滅菌和 ETO 滅菌。PTFE 對高壓滅菌循環具有極佳的耐溫能力,而對 ETO 的快速通氣吸收能力則極低,因此非常適合使用多種滅菌方法的設備。
問:排氣塞可以承受多少次消毒週期?
A: 高品質的 PTFE 通風塞通常可承受 100 次以上的高壓滅菌循環或 50 次以上的 ETO 循環,同時保持過濾性能。實際循環壽命取決於滅菌參數、處理程序以及您特定應用的性能驗收標準。
問:醫療應用中的無菌過濾需要多大的孔徑?
A: 醫療應用通常需要 0.2 或 0.22 微米的孔徑,以達到可靠的細菌截留效果。這種孔徑可提供經驗證的無菌保證,同時允許足夠的氣流,以達到有效的殺菌和壓力平衡。
問:可消毒的排氣塞是否需要特殊的驗證測試?
A: 是的,可滅菌通風塞需要進行驗證測試,包括熱性能、微生物挑戰和材料相容性研究。測試必須遵循 FDA 指南和 ISO 標準,並提供相關文件,以支援您的滅菌製程驗證和法規申請。
問:如何防止滅菌過程中的排氣塞污染?
A: 透過正確的安裝、處理時的保護蓋、經驗證的滅菌參數和滅菌後的適當儲存來防止污染。安裝時請使用無菌技術,並確保排氣塞的設計符合您特定的滅菌方法和應用要求。


